Blog

Vamos falar sobre radiografia industrial
12 de dezembro de 2022
Tempo de leitura: 6 minuto(s)
Hoje falaremos das diferenças entre o Raio-x e o raio Gama (Gamagrafia)
Mas antes, porém, precisamos entender um pouco essa questão de radiação.
Descrição Genérica do Método e Aplicações
A Radiografia Industrial é um método usado para inspeção não destrutiva que se baseia na absorção diferenciada da radiação penetrante pela peça que está sendo inspecionada. Devido às diferenças na densidade e variações na espessura do material, ou mesmo diferenças nas características de absorção causadas por variações na composição do material, diferentes regiões de uma peça absorverão quantidades diferentes da radiação penetrante.
Essa absorção diferenciada da radiação poderá ser detectada através de um filme, ou através de um tubo de imagem ou mesmo medida por detectores eletrônicos de radiação.
Essa variação na quantidade de radiação absorvida, detectada através de um meio, irá nos indicar, entre outras coisas, a existência de uma falha interna ou defeito no material.
A Radiografia Industrial é então usada para detectar variação de uma região de um determinado material que apresenta uma diferença em espessura ou densidade comparada com uma região vizinha, em outras palavras, a radiografia é um método capaz de detectar com boa sensibilidade defeitos volumétricos.
Isto quer dizer que a capacidade do processo de detectar defeitos com pequenas espessuras em planos perpendiculares ao feixe, como trinca dependerá da técnica de ensaio realizado. Defeitos volumétricos como vazios e inclusões que apresentam uma espessura variável em todas as direções, serão facilmente detectadas desde que não sejam muito pequenos em relação à espessura da peça.

Natureza da Radiação Ionizante
Com a descoberta do Raio-X pelo físico W. C. Roentgen em 1895, imediatamente iniciaram-se os estudos sobre as emissões de partículas, provenientes de corpos radioativos, observando suas propriedades e interpretando os resultados.
Nesta época, destacaram-se dois cientistas, Pierre e Marie Curie, pela descoberta do polônio e o radium e ainda deve-se a eles a denominação “Radioatividade” (propriedade de emissão de radiações por diversas substâncias).
No começo do século XX, 1903, Rutherford, após profundos estudos formulou hipóteses sobre as emissões radioativas, pois convém frisar, que naquela época ainda não se conhecia o átomo e os núcleos atômicos e coube a este cientista a formulação do primeiro modelo atômico criado e que até hoje permanecem suas características.
O nome “Radiação Penetrante” se originou da propriedade de que certas formas de energia radiante possuem de atravessar materiais opacos à luz visível.
Podemos distinguir dois tipos de radiação penetrante usados em radiografia industrial: os Raios X e os Raios Gama.
Eles se distinguem da luz visível por possuírem um comprimento de onda extremamente curto, o que lhes dá a capacidade de atravessarem materiais que absorvem ou refletem a luz visível.
Por serem de natureza semelhante à luz, os Raios X e os Raios Gama possuem uma série de propriedades em comum com a luz entre as quais podemos citar: possuem a mesma velocidade de propagação (300.000 km/s), deslocam-se em linha reta, não são afetadas por campos elétricos ou magnéticos, possuem a propriedade de impressionar emulsões fotográficas. Poderíamos citar outras propriedades comuns entre as radiações penetrantes e a luz visível.
Ocorre, no entanto, que vários fenômenos que observamos na luz, são muitos difíceis de serem detectados. O fenômeno de refração, por exemplo, ocorre nas radiações penetrantes, mas numa escala tão pequena que são necessários instrumentos muito sensíveis para detectá-lo. Isso explica porque a radiação penetrante não pode ser focalizada através de lentes, como acontece com a luz.
No âmbito dos Ensaios Não Destrutivos devemos salientar seis propriedades da radiação penetrante que são de particular importância:
- Deslocam-se em linha reta;
- Podem atravessar materiais opacos a luz, ao fazê-lo, são parcialmente absorvidos por esses materiais;
- Podem impressionar películas fotográficas, formando imagens;
- Provocam o fenômeno da fluorescência;
- Provocam efeitos genéticos;
- Provocam ionizações nos gases.

Estrutura da Matéria:
Em 1906, Ernest Rutherford realizou experiências com bombardeio de partículas alfa em finas folhas de ouro (as partículas alfas são emitidas por certos radioisótopos, ocorrendo naturalmente). Ele achava que a maioria das partículas passavam direto através da fina folha do metal em sua direção original. Contudo, algumas partículas foram desviadas.
Experiência atômica de Rutherford em 1906. Isto levou ao desenvolvimento do modelo atômico que é aceito até hoje. O núcleo contém carga positiva do átomo e ao redor do núcleo, giram um número de elétrons.
Os elétrons ocupam níveis ou camadas de energia e o espaçamento desses níveis causam o grande tamanho do átomo em comparação com o núcleo.
- Núcleo
- camada K
- camada L
- camada M
- Modelo atômico de Rutherford.
Os cientistas conheciam agora que o átomo consistia em um núcleo contendo um número de prótons e uma nuvem eletrônica com igual número de elétrons. Contudo eles achavam confuso, pelo fato do átomo de hélio (número atômico 2) pesar quatro vezes mais que o átomo de hidrogênio. Irregularidades no peso persistiam através da tabela periódica. Predisseram algumas teorias para o acontecido, mas a confusão terminou em 1932, quando James Chadwick, físico inglês, descobriu uma partícula chamada de nêutron.
Essa partícula tinha uma massa igual ao do próton, mas não tinha carga. Para descrever essa nova propriedade, cientistas alegaram o número de massa, número de partículas (prótons e nêutrons no núcleo). Descrevendo o átomo, o número de massa seria escrito com um número superior no símbolo químico.
Variações e Composição dos Átomos, Radioisótopos:
Todos os elementos que contém, em seu núcleo atômico, o mesmo número de prótons, mas que possuem números diferentes de nêutrons, manifestam as mesmas propriedades químicas e ocupam o mesmo lugar na classificação periódica.
São elementos que, por terem o mesmo número de prótons, têm o mesmo número atômico e por terem números diferentes de nêutrons têm número de massa diversos. São chamados isótopos, nome cuja etnologia indica o mesmo lugar que ocupam na classificação periódica dos elementos.
O número de isótopos conhecidos, de cada elemento, é muito variável. O Iodo, por exemplo, tem 13, o ferro e o Urânio têm 6, cada um. Os isótopos de um mesmo elemento não têm as mesmas propriedades físicas. Assim, por exemplo, o isótopo do Iodo (I-127) é estável, todos os outros são radioativos, isto é, são chamados de radioisótopos.
A partir de 1954, os radioisótopos passaram a ser produzidos em escala apreciável, nos reatores, iniciando-se a fase de produção de fontes radioativas de alta intensidade que têm um grande número de aplicações industriais.
Os trabalhos baseados no emprego dos radioisótopos têm hoje enorme extensão. As experiências multiplicaram-se em muitos setores e, não é exagero dizer que os radioisótopos têm trazido uma verdadeira revolução em todos os domínios, nos quais a experimentação desempenha papel preponderante.

Radiação e Radioatividade
Define-se “Radioatividade” como sendo a emissão espontânea de radiação por um núcleo atômico, que se encontra num estado excitado de energia.
Existem três tipos diferentes de radiação, como segue:
- Partículas Alfa (a)
- Partículas Beta (b)
- Raios Gama (g)
As partículas “Alfa” são constituídas de dois nêutrons e dois prótons, caracterizando um núcleo atômico de Hélio. Devido ao seu alto peso e tamanho, elas possuem pouca penetração e são facilmente absorvidas por poucos centímetros de ar.
As partículas “Beta” são constituídas por elétrons, que possuem velocidades próximas da luz, com carga elétrica negativa. Possuem um poder de penetração bastante superior às radiações Alfa, podendo ser absorvidas por alguns centímetros de acrílico ou plásticos, na sua grande maioria. As “partículas” “Gama” são de natureza ondulatória, ao contrário das demais que tem características corpusculares. Devido a isto, adquire um alto poder de penetração nos materiais.
E possível separar os três tipos de radiação descritos através da aplicação de um campo elétrico ou magnético, numa amostra de material radioativo.
Esquema de separação das radiações alfa, beta e gama
O poder de penetração das radiações eletromagnéticas, Raios X e Gama, são caracterizadas pelo seu comprimento de onda (ou energia). As propriedades dos Raios X que tem importância fundamental, quando se trata de ensaios não destrutivos e são aquelas citadas anteriormente.
Outras grandezas relativas às ondas eletromagnéticas são frequência e energia. Podemos converter a energia em comprimento de onda ou em frequência.
A equação que relaciona a energia com o comprimento de onda é a equação de Planck:
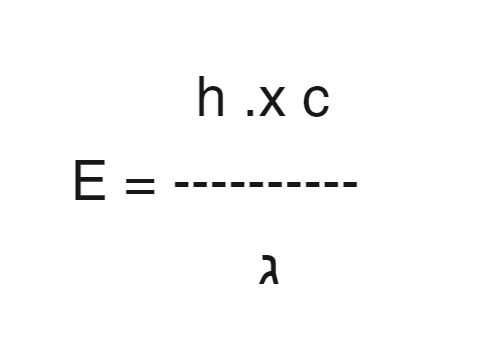
Algumas diferenças entre o Raio-x e o raio gama (Gamagrafia)
Aparelhos de Raio-X:


- Precisam de energia elétrica para funcionar,
- Em geral são maiores e mais pesados dificultando os serviços de campo,
- Tem controle de kV e mA, podendo variar a qualidade da radiação,
- Podem ser transportados como qualquer equipamento, pois não emite radiação sem energia elétrica,
Aparelhos de Gama (Gamagrafia):


- Não precisam de energia elétrica para funcionar,
- Proporcionam mais agilidade na hora de executar os arranjos radiográficos, principalmente em locais de difícil acesso em comparação aos aparelhos de RX.
- Em geral tem um grande poder de penetração podendo radiografar grandes espessuras de aço e outros materiais.
- O transporte deve ser feito com muito cuidado, seguindo as normas e procedimentos.
Quanto as técnicas radiográficas e o processamento dos filmes não mudam nada, os profissionais seguem os procedimentos próprios de cada norma, efetuando os cálculos de acordo com os equipamentos usados, tipo de material, espessura, distância fonte/filme etc.
